Mikä rooli pyrimidiinijohdannaisilla on biologisissa järjestelmissä?
Nov 07,2025Kuinka triatsiinijohdannaiset toimivat antimikrobisina tai sienilääkkeinä?
Oct 24,2025Mikä tekee karbatsolijohdannaisista kemiallisesti stabiileja?
Oct 17,2025Kuinka karbatsolijohdannaiset käyttäytyvät happamissa tai emäksisissä olosuhteissa
Oct 10,2025Voidaanko furaanijohdannaisia valmistaa uusiutuvasta biomassasta?
Oct 03,2025Pyridiinijohdannaiset ovat luokka orgaanisia yhdisteitä, jotka ovat saaneet merkittävän huomion lääkekemian valtakunnassa, pääasiassa niiden monipuolisten vuorovaikutusten kanssa biologisten järjestelmien kanssa. Pyridiinin, kuuden jäsenen heterosyklisen yhdisteen, joka sisältää typpeä sisältävän heterosyklisen yhdisteen, ainutlaatuisia rakenteellisia ominaisuuksia, jotka mahdollistavat sen johdannaiset erilaisten biomolekyylisten kohteiden kanssa. Tämä monipuolisuus tekee pyridiinijohdannaisten arvokkaat työkalut lääkekehityksessä, etenkin neurologisten, sydän- ja verisuoni- ja tartuntatautien hoidossa.
Näiden vuorovaikutusten ytimessä on typpiatomi pyridiinirenkaassa, jolla on keskeinen rooli sitoutumisaffiniteetin välittämisessä biologisiin reseptoreihin. Typen elektronegatiivisuus mahdollistaa pyridiinijohdannaisten muodostaa vety sidoksia ja koordinoida metalli -ionien kanssa, vuorovaikutukset, jotka ovat välttämättömiä niiden biologisen aktiivisuuden kannalta. Seurauksena on, että nämä yhdisteet voivat moduloida entsymaattisia funktioita, vaikuttaa reseptorin signalointiin ja jopa muuttaa geeniekspressiota.
Pyridiinijohdannaisten vuorovaikutus entsyymien kanssa on yksi niiden biologisen aktiivisuuden hyvin tutkituimmista puolista. Monet pyridiinipohjaiset yhdisteet toimivat keskeisten entsyymien, kuten kinaasien, fosfataasien ja asetyylikolinesteraasien estäjinä tai aktivaattoreina. Sitoutumalla näiden entsyymien aktiivisiin kohtiin pyridiinijohdannaiset voivat joko estää tai parantaa niiden aktiivisuutta, mikä johtaa terapeuttisiin tuloksiin. Esimerkiksi asetyylikoliiniesteraasin estämisellä pyridiinijohdannaisilla on keskeinen rooli Alzheimerin taudin hoidossa, jossa tavoitteena on lisätä asetyylikoliinitasoja, muistiin ja kognitioon osallistuvaa välittäjäainetta.
Lisäksi pyridiinijohdannaisilla on usein selektiivinen sitoutuminen spesifisiin reseptoreihin, mukaan lukien G-proteiiniin kytketyt reseptorit (GPCR) ja ionikanavat, jotka ovat mukana solun signalointiprosesseissa. Heidän kykynsä olla vuorovaikutuksessa näiden reseptoreiden kanssa tekee heistä potentiaalisia ehdokkaita neurologisiin häiriöihin kohdistuvien lääkkeiden, kuten masennuksen, skitsofrenian ja Parkinsonin taudin, kehittämiseen. Pyridiinijohdannaisten kyky moduloida välittäjäaineiden vapautumista ja reseptoreiden aktivaatiota tai estämistä on niiden farmakologisen profiilin kulmakivi.
Heidän suoran vuorovaikutuksensa lisäksi entsyymien ja reseptoreiden kanssa pyridiinijohdannaiset voivat myös vaikuttaa geeniekspressioon. Useat tutkimukset ovat osoittaneet, että nämä yhdisteet voivat vaikuttaa tiettyjen geenien transkriptionaaliseen aktiivisuuteen vuorovaikutuksessa ydinreseptoreiden tai muiden transkriptiotekijöiden kanssa. Tämä kyky moduloida geeniekspressio avaa uusia tapoja pyridiinipohjaisten terapioiden kehittymiselle, joiden tavoitteena on hoitaa olosuhteita, kuten syöpä, jossa spesifisten geenien säätely on ratkaisevan tärkeä kasvaimen etenemiselle ja etäpesäkkeelle.
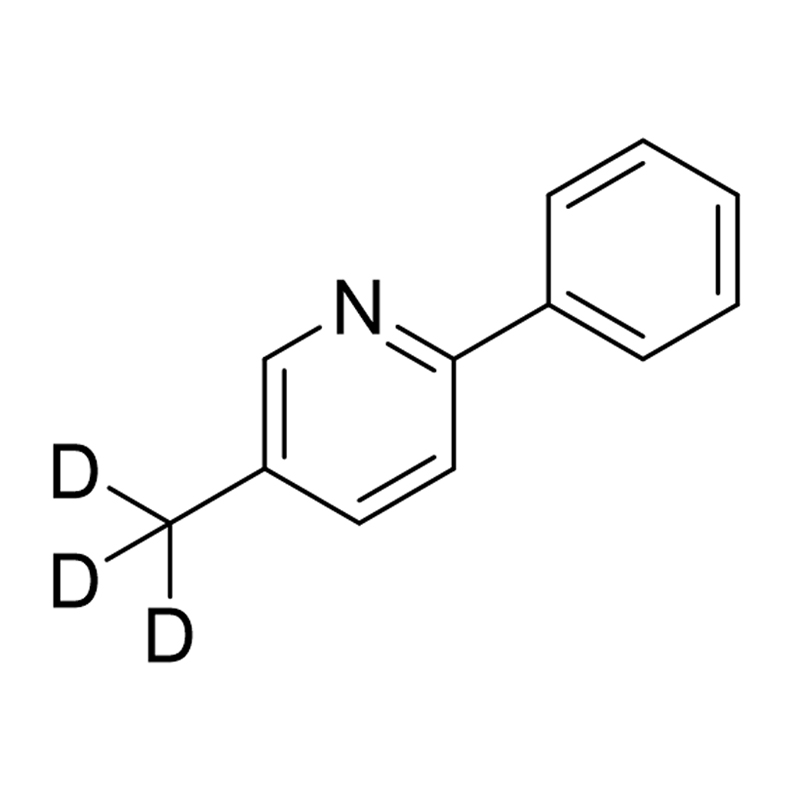
Eentsymaattisten ja reseptorivuorovaikutusten lisäksi pyridiinijohdannaiset tunnetaan kyvystään kelatoida metalli -ioneja, ominaisuus, jota voidaan hyödyntää syöpälääkkeiden suunnittelussa. Sitoutumalla metalli -ioneihin, kuten sinkkiin, kupariin tai rautaan, pyridiinijohdannaiset voivat häiritä metalloproteiinien ja entsyymien toimintaa, jotka luottavat näihin metalleihin niiden aktiivisuuden suhteen. Tämä kelaatio voi johtaa kriittisten biologisten prosessien, kuten DNA: n korjaamisen, solujen jakautumisen ja apoptoosin, häiriöihin, mikä tekee pyridiinijohdannaisista tehokkaita syövän ja muiden sairauksien hoidossa.
Lisäksi pyridiinijohdannaisten farmakokinetiikka, mukaan lukien niiden absorptio, jakautuminen, aineenvaihdunta ja erittymisprofiilit, ovat kriittisiä tekijöitä niiden tehokkuuden määrittämisessä terapeuttisina aineina. Monien pyridiinijohdannaisten lipofiilinen luonne antaa heille mahdollisuuden ylittää biologiset kalvot helposti, mikä tekee niistä sopivia ehdokkaita suun kautta annettavaksi. Pyridiinirakenteen muutokset voivat kuitenkin vaikuttaa niiden liukoisuuteen, stabiilisuuteen ja puoliintumisaikaan, mikä vaatii huolellista optimointia lääkkeen suunnitteluprosessin aikana.
Pyridiinijohdannaisten toksikologinen profiili on toinen tärkeä osa niiden vuorovaikutusta biologisten järjestelmien kanssa. Vaikka monilla pyridiinijohdannaisilla on lupaava terapeuttinen potentiaali, niiden toksisuus voi rajoittaa niiden kliinisiä sovelluksia. Myrkyllisyys johtuu usein niiden vuorovaikutuksesta kohteen ulkopuolisten proteiinien kanssa tai metaboliittien kertymisestä, jotka häiritsevät normaalia solun toimintaa. Näin ollen näiden myrkyllisten vaikutusten taustalla olevien molekyylimekanismien ymmärtäminen on välttämätöntä turvallisempien pyridiinipohjaisten lääkkeiden kehittämiseksi.
Pyridiinijohdannaiset ovat monipuolinen ja dynaaminen ryhmä yhdisteitä, jotka ovat yhteydessä biologisiin järjestelmiin monien mekanismien kautta. Entsyymin estämisestä ja reseptorimodulaatiosta geeniekspressioon ja metallikelaatioon näillä yhdisteillä on valtava lupaus uusien terapeuttisten aineiden kehittymiselle. Heidän koko potentiaalinsa voidaan kuitenkin toteuttaa vain jatkamalla heidän toimintamekanismeja, farmakokinetiikkaa ja turvallisuusprofiileja. Lääkekemian jatkuvilla edistymisillä pyridiinijohdannaiset ovat valmiita olemaan entistä merkittävämpi rooli monenlaisten sairauksien hoidossa.

